La inspección visual consiste en encontrar productos defectuosos y eliminarlos del proceso de producción. Podemos realizar la inspección visual de forma manual o automática con sistemas de cámaras. Muchas empresas utilizan la inspección visual automática por diferentes motivos, normalmente para reducir costes, mejorar la detección, aumentar el rendimiento de la producción, satisfacer las demandas del mercado o incluso mejorar la reputación de la marca.
 |
 |
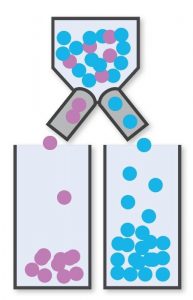
Lo idealEl objetivo de los sistemas de inspección y clasificación es clasificar los productos de forma inequívoca en grupos según los requisitos de clasificación. Lo ideal es que los sistemas de inspección sean una combinación de hardware y software totalmente ajustables que puedan configurarse para manejar todo tipo de productos y detectar y eliminar toda clase de defectos visuales. En la producción farmacéutica hay muchos tipos de defectos (de comprimidos, cápsulas, cápsulas blandas, viales, jeringas, etc.) y cada producto tiene su propia apariencia con defectos visuales concretos. Además, los requisitos para la clasificación de defectos visuales no están estandarizados en la industria. Por ejemplo, una determinada variación de color del producto podría considerarse un defecto para una empresa, pero no para otra empresa similar al otro lado de la calle. Para satisfacer los requisitos del usuario, los sistemas de inspección suelen tener muchos parámetros que configurar, lo que conlleva un alto riesgo de funcionamiento subóptimo o inadecuado. Por esa razón, deberían diseñarse sistemas de inspección que escondan su complejidad y hagan que la tecnología sea fácil de usar incluso para los no expertos. Los sistemas de inspección perfectamente diseñados son ajustables para diferentes productos y tipos de defectos (flexibles), capaces de detectar defectos con precisión (sensibles) y, por último, pero no menos importante, inteligentes para distinguir correctamente los defectos de las desviaciones aceptables (selectivos). Buscar la máxima sensibilidad y selectividad al mismo tiempo es donde lo ideal se mezcla con la realidad. |
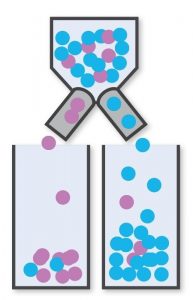
La realidad¿Recuerda lo molesto que es cuando una máquina no funciona tan bien como esperaba? Las dos razones más comunes de decepción con la tecnología de inspección son las expectativas poco realistas de sensibilidad, es decir, la capacidad de detectar defectos, y la selectividad, que es una palabra elegante para referirse a la capacidad de tener una baja tasa de rechazo de buenos productos. El error más frecuente es pensar que instalar un sistema con una cámara de alta resolución hace que la inspección sea muy sensible y selectiva. Sin embargo, la sensibilidad del sistema de inspección depende de muchos parámetros que no siempre son obvios. El parámetro óptico no es solo la resolución, sino también el ruido de la cámara, la homogeneidad de la luz, la distorsión de la lente, etc. Además, en los sistemas de inspección visual hay algo más que parámetros ópticos. Igualmente importantes son la estabilidad y repetibilidad del manejo mecánico del producto y el correcto análisis de la imagen. Un diseño defectuoso o imperfecto en solo uno de los segmentos del sistema de inspección puede generar una mayor incertidumbre en la medición y, por lo tanto, menores tasas de detección y aumento de la tasa de rechazo de buenos productos. Además, la tasa de rechazo es un compromiso entre la sensibilidad y la susceptibilidad a errores, la selectividad. Y, como el rechazo supone una pérdida directa para el negocio, se cuestiona a diario en los procesos de producción. Solo cuando tratamos de optimizar el proceso de producción reconocemos el verdadero valor del sistema de inspección elegido. |